Um sistema conjugado é aquele em que possa ocorrer deslocalização eletrônica em ligações covalentes. Ao fazer isso, a conjugação diminui a energia total da molécula, sendo muito importante no entendimento da reatividade, estabilidade e propriedades de muitas espécies.
A ressonância ocorre em estruturas em que a ligação π pode ser rearranjada para formar estruturas equivalentes. A representação mais próxima da realidade se dá pelo híbrido de ressonância, que é a média de todas as estruturas equivalentes possíveis, ou contribuintes de ressonância. Por exemplo, a molécula de ozônio é melhor representada por:
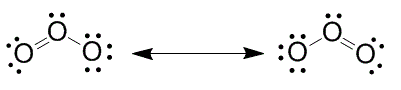
Isso não é um equilíbrio. Não há ozônio em duas maneiras diferentes, mas em apenas uma forma híbrida entre cada contribuição individual.
O híbrido de ressonância não é a descrição completa das ligações da molécula, mas uma maneira de racionalizá-las através de um modelo acessível. A contribuição de cada estrutura no híbrido não pode ser observada experimentalmente já que é uma mera abstração.
Assim como no efeito indutivo, a ressonância também pode aumentar ou diminuir a densidade eletrônica em uma molécula, sendo um efeito muito mais intenso que o indutivo.
Grupos Retiradores de Densidade Eletrônica
Os principais grupos que retiram densidade eletrônica por ressonância são: -NO2, -CN, -HSO3.
Grupos Doadores de Densidade Eletrônica
Os principais grupos que doam densidade eletrônica por ressonância são: -OMe (éteres em geral), -NR2 (aminas em geral), -OH (em aromáticos).
Evidências Físicas
A distância de uma ligação química pode ser medida pela distância entre seus núcleos, e a técnica de Raios-X é capaz de realizar essa medida. Como ligações simples são mais longas que as duplas, se a ressonância não ocorresse era de se espera diferentes comprimentos de ligação para o ozônio e benzeno.
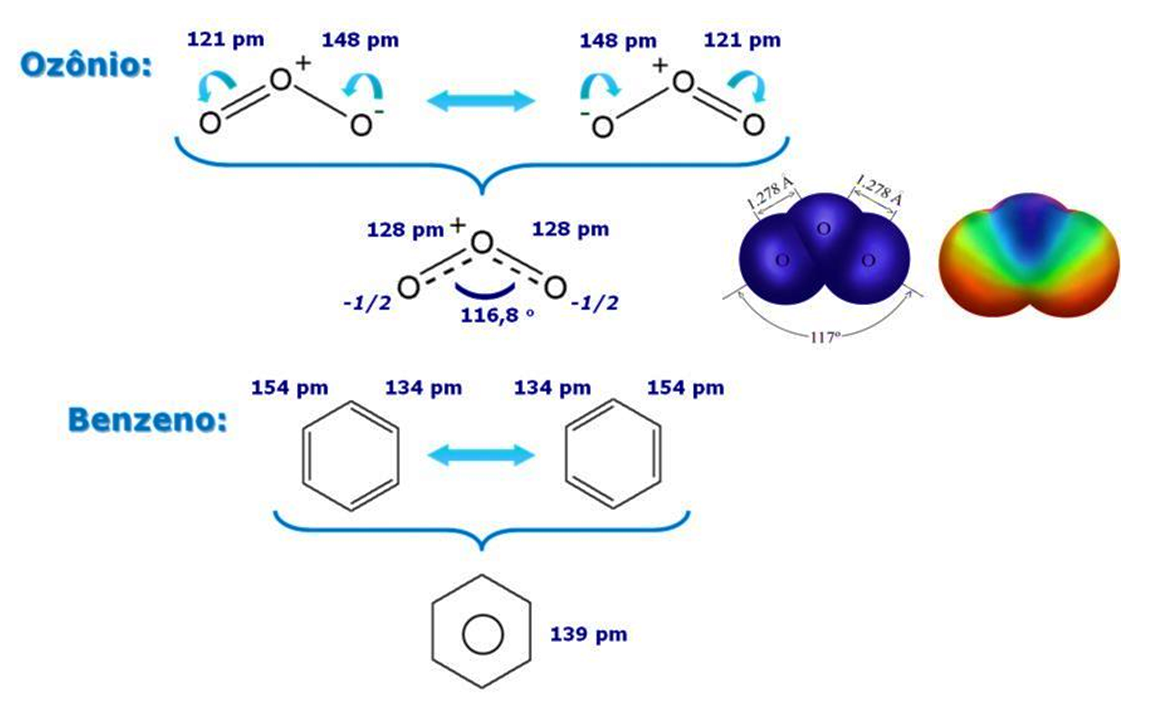
Entretanto, não é isso o que se verifica experimentalmente. O que é observado é um comprimento de ligação intermediário entre simples e dupla, de modo que o hibrido de ressonância é a maneira mais próxima que há para representar tais ligações.
