A eletronegatividade é uma medida de atração eletrônica derivada da Afinidade Eletrônica. Ela mede o quanto um elemento irá atrair para seu núcleo a densidade eletrônica da ligação química. Para os elementos representativos e de modo geral, a eletronegatividade aumenta para direita no mesmo período e para cima na mesma família, sendo a eletronegatividade decrescente F > O > N ~ Cl. Os metais de transição sofrem fenômenos (como a Contração dos Lantanídeos) que não permitem grande generalização.
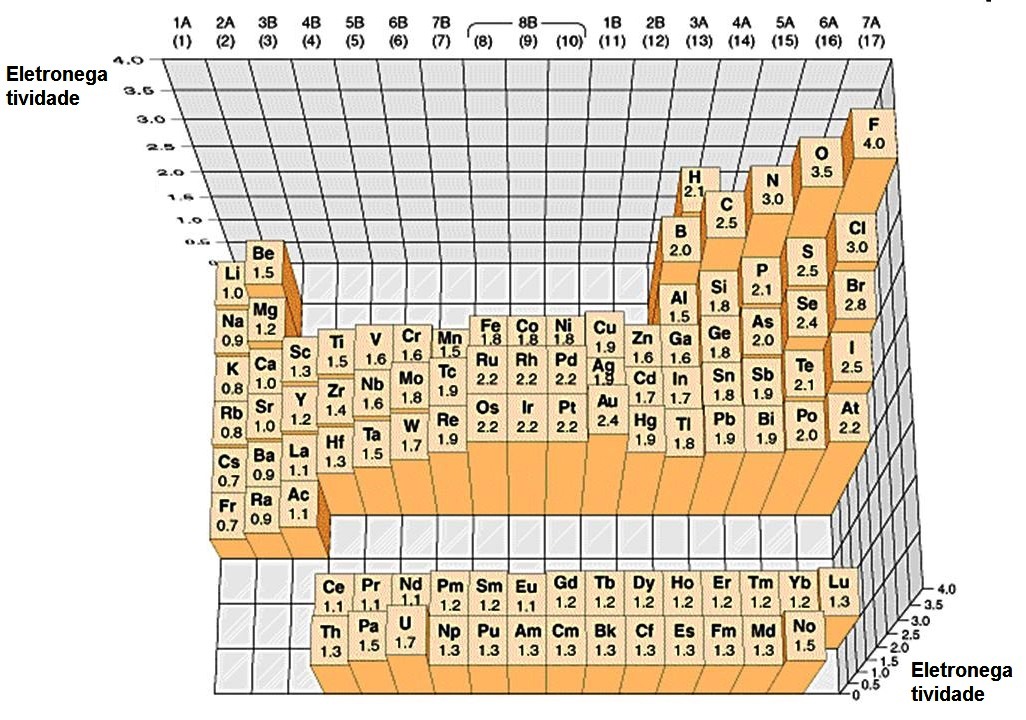
Para obter uma Tabela Periódica com os valores de eletronegatividade clique aqui.
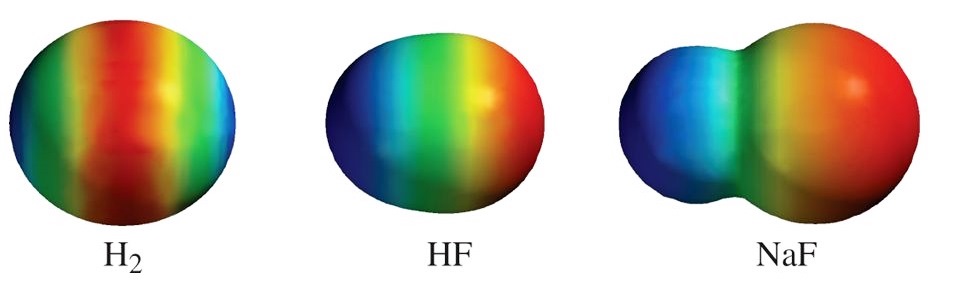
Moléculas diatômicas homonucleares como o H2, N2, O2 e Cl2 possuem tendência simétrica da distribuição eletrônica, pois seus constituintes possuem exatamente a mesma eletronegatividade. Em moléculas heteronucleares como HF ou BrCl os constituintes possuem diferentes eletronegatividades, logo a densidade eletrônica tende a se deslocar para o núcleo mais eletronegativo. Em moléculas em que a diferença de eletronegatividade é pequena, como no CH4, esse efeito é presente mas pouco pronunciado.
A tendência da nuvem eletrônica em ficar mais próxima ao núcleo mais eletronegativo produz distorções locais de carga, o que afeta profundamente as propriedades da molécula.