A geladeira é um dos itens domésticos mais indispensáveis. Como ela é capaz de transformar a eletricidade em temperaturas congelantes?
Por Carlos Vinícius Pinto dos Santos

Figura 1 - Apesar do processo de resfriamento ser um fenômeno físico seu estudo também ocorre na química atraves do campo da físico-química
A geladeira utiliza fenômenos de compressão e descompressão de gases, que são tradicionalmente estudados pela física, para criar diferença de temperatura entre duas regiões. Entretanto, a Físico-Química (que é uma área de fronteira entre a Química e a Física) também estuda esses mesmos fenômenos, mas com ênfase no comportamento molecular e suas interações durante tais processos.
O princípio envolvido é o da expansão do gás contido na tubulação da geladeira. O motor utiliza a eletricidade para comprimir o gás e aumentar sua pressão e, consequentemente, sua temperatura pelo aumento dos choques mecânicos entre as moléculas. O gás quente passa pelo radiador que troca calor com o ambiente, resfriando o gás contido. A tubulação é em forma de zig-zag para otimizar a troca de calor e, após resfriar, o gás se liquefaz sob alta pressão.
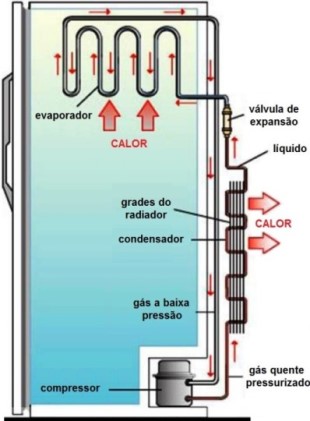
Figura 2 - Funcionamento básico de um refrigerador doméstico
A válvula de expansão controla a entrada do líquido no evaporador, que tem sua pressão diminuída, permitindo assim sua vaporização. Como esse é um processo endotérmico, a temperatura dos arredores diminui para cerca de -19ºC1. Pode existir ainda um evaporador secundário para permitir que as geladeiras com o compartimento do congelador isolado (geladeira duplex) tenham temperaturas baixas, porém mais altas do que as obtidas no congelador, no compartimento maior.
Como o processo conduzido pela geladeira não é espontâneo, o isolamento é um fator crucial para minimizar as trocas de calor com o ambiente externo. Toda a geladeira é revestida por pelo menos duas camadas de isolamento: o poliestireno resistente à óleos na parte interna, que fica em contato com o ambiente da geladeira, e materiais isolantes entre o plástico e as chapas metálicas externas. Os materiais isolantes mais usados são lã de vidro e espuma de poliuretano. A lã de vidro oferece ótimo isolamento, mas pode oferecer riscos ao manuseio inadequado por provocar micro ferimentos na pele, enquanto que o poliuretano libera gás cianídrico (HCN) e cianogênio (CN2) durante sua combustão. Para um equipamento elétrico, que naturalmente está sujeito a incêndio, isso deve ser levado em consideração na alocação do eletrodoméstico, sendo preferido um local ventilado.
A diferença de temperatura entre o meio interno e o externo é diretamente proporcional à eficiência. Por isso que não se deve obstruir a passagem de ar na grade metálica, seja por manter a geladeira em um local pouco ventilado, seja por colocar objetos na grade do radiador. Se isso ocorrer, a eficiência do processo é diminuída, demandando mais tempo e ciclos do compressor para alcançar a temperatura desejada, aumentando significativamente o consumo de energia.
Gás Refrigerante
No início do século XX, os gases refrigerantes mais utilizados eram a amônia (R-717), o clorometano (R-40) e o dióxido de enxofre (R-764). Mas, devido a uma série de acidentes que causaram sérias consequências uma alternativa foi descoberta pela Frigidaire em 1928: chamado genericamente de freon (ou CFC de clorofluorocarbonetos), são substâncias gasosas compostas de carbono, flúor, hidrogênio e outro halogênio, geralmente o cloro, com excelentes características químicas e físico-químicas. A partir de então os CFC tornaram os refrigerantes anteriores obsoletos e tomaram o mercado, também sendo usados como veículos para aerossóis.
Entretanto, a estabilidade química dos compostos na baixa atmosfera não se reproduzia na estratosfera, onde raios ultravioleta de alta energia incidem. A energia de ligação de C-Cl é de 397kJ/mol2, contra 536kJ/mol2 da ligação C-F, e uma das faixas de radiação UV incidente é a UVC de 100-279nm (ou 12,4-4,43 eV) com energia suficientemente forte para produzir cloro atômico a partir dos CFC. Esse cloro então pode atacar uma molécula de ozônio para gerar oxigênio e monóxido de cloro, que reage novamente com o ozônio para gerar oxigênio e restabelecer o cloro.
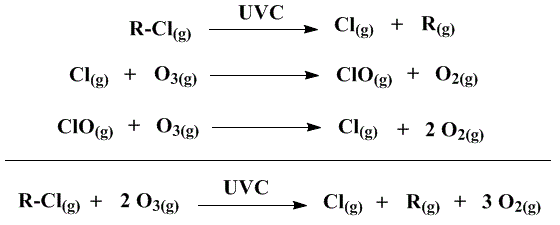
Esquema 1 - Processo de fotodegradação de substâncias organocloradas
Devido aos possíveis impactos ambientais foram assinados acordos mundiais para diminuir drasticamente a emissão de CFC na atmosfera. A solução foi substituir o cloro por flúor tornando a molécula mais estável e restringir seu uso aos refrigeradores de ciclo fechado. O CFC foi substituído por uma mistura de propano/butano como propelente para aerossóis.
Atualmente, vários polifluoridrocarbonetos, ou HFC, são utilizados em substituição aos CFC. Um dos mais comuns é o R134a, se tratando do 1,1,1,2-tetrafluoroetano.
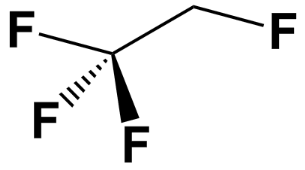
Figura 3 - Estrutura química do refrigerante R134a
Refrigeradores de Absorção
Leo Szilard e Albert Einstein inventaram um refrigerador à base de amônia e butano em 1930.
A geladeira proposta não tem partes móveis, causa de alguns acidentes no início do século XX e não necessita de energia elétrica para operar, sendo necessário apenas de uma fonte de calor como um pequeno queimador de gás. O circuito do fluxo de água serve como uma bomba de amônia e o circuito do fluxo de amoníaco serve como uma bomba de butano. O sistema amônia/água é uma escolha apropriada já que a amônia é altamente solúvel em água e sua solubilidade diminui acentuadamente com o aumento da temperatura. Por outro lado, o butano é uma escolha apropriada para o refrigerante, pois tem um ponto de ebulição adequadamente baixo e é praticamente insolúvel em água.
Em uma geladeira normal, a parte fria se dá pela evaporação do fluido refrigerante condensado. Na geladeira de Sczilard, o líquido refrigerante evapora por diferença de pressão parcial, sendo arrastado pelo fluxo de amônia que, quando entra em contato com a água, libera o butano que alimenta o ciclo. A parte quente, numa geladeira comum, é o conjunto compressor e radiador, sendo o primeiro o que comprime o gás e o segundo o que arrefece o gás recém-comprimido para torná-lo líquido. Na geladeira de Sczilard, as partes quentes ocorrem no aquecimento da mistura amônia/água, para restaurar a amônia no ciclo e o aquecimento da água que entrará em contato com a mistura amônia/ butano.
O fluido refrigerante condensado não se dissolve em água e, no caso de butano, por ser menos denso irá flutuar facilitando a separação para o evaporador. Enquanto isso, a solução de amoníaco/água flui para um gerador de amoníaco, em que o calor fornecido por uma fonte externa qualquer que expulsa a amônia para o evaporador, reiniciando o processo.
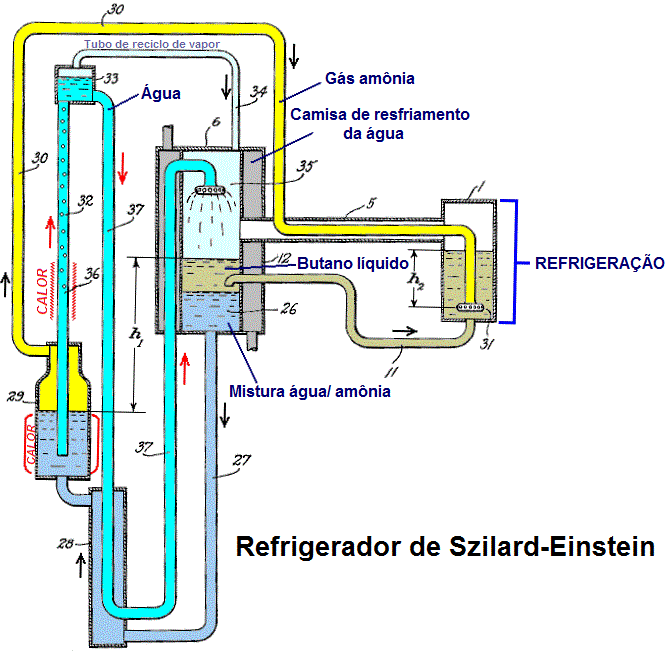
Figura 4 - Funcionamento do refrigerador de Szilard-Einstein
Algumas empresas já comercializam refrigeradores com compressor para gás carbônico mas, por enquanto, apenas para uso industrial. Segue abaixo a diferença nas dimensões entre um compressor para CO2 e outro para fluorocarbonetos (ou HFC).

Figura 5 - Motores de refrigeração à CO2 (gás carbônico)
Os refrigeradores de CO2 são utilizados apenas a nível industrial/ comercial, principalmente por conta das pressões elevadas exigidas. Funcionam também com base nas mudanças de estado, seja subcrítico ou transcrítico3. Apesar de não ser uma tecnologia nova, seu uso foi negligenciado pelo advento dos CFC, mas há projetos para uso em ar condicionados e outros refrigeradores menores, com potencial uso residencial. Segue abaixo um esquema geral do funcionamento do sistema.
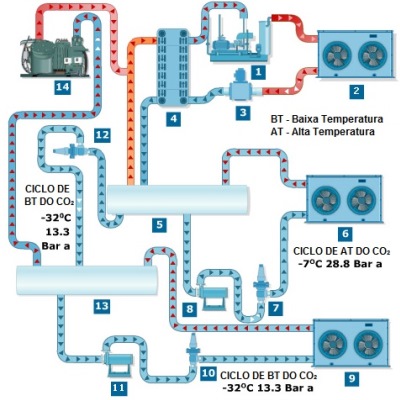
Figura 6 - Funcionamento do refrigerador de gás carbônico
O diagrama de fases do CO2 demonstra as possíveis dificuldades técnicas de sua implantação em larga escala. Lembrando que 1 bar = 1,02 atm e que T(ºC) = T(K) - 273,15K.
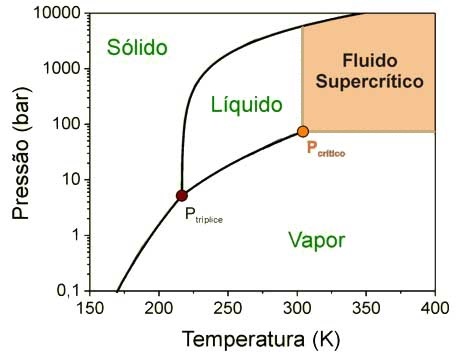
Figura 7 - Diagrama de fases do gás carbônico
Quem diria que há tanta Química envolvida com os processos de resfriamento das geladeiras? Continue explorando a Química conosco com nossas sugestões ao fim da página.
Referências
1 Portal do Professor - Máquina térmica (geladeira)
3 CO2 As Refrigerant: The Transcritical Cycle
