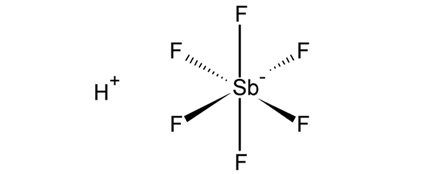
Apesar de a teoria de Arrhenius ter sido bem aceita por bioquímicos e fisiologistas, houve muita resistência por sua adoção entre os Químicos. Houve muitas críticas à teoria, como a não aplicabilidade em sistemas não aquosos e alguns casos aquosos (neutralização de amônia em ácidos aquosos), além das críticas dos alemães Paul Pfeiffer e Alfred Werner, pertinentes a sistemas de coordenação.
Em 1923 foi proposta, simultanea e independentemente, uma nova teoria ácido-base pelo dinamarquês Johannes Nicolaus Brønsted1, pelo inglês Thomas Martin Lowry e pelo estadunidense Gilbert Newton Lewis, em ordem decrescente de contribuição. Em comparação à teoria de Arrhenius, é mantida a característica do ácido que gera um íon hidrogênio - que essencialmente é um próton - e por isso também é chamada de teoria protônica. Entretanto, a diferença reside na base que pode ser qualquer substância capaz de receber esse próton e não mais na substância que gera a hidroxila.
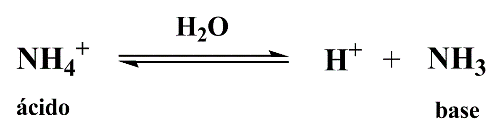
Dessa forma, a água pode atuar como base frente a qualquer ácido mais forte que ela, produzindo o ácido conjugado H3O+ relatado por Latimer e Rodebush em 19202. Vários estudos posteriores investigaram a aglomeração de várias moléculas de água para equilibrar a carga do H+, formando estruturas com diferentes quantidades de moléculas de água3. Para efeito prático, será levado em consideração apenas o aglomerado mais simples, o hidrônio - H3O+.
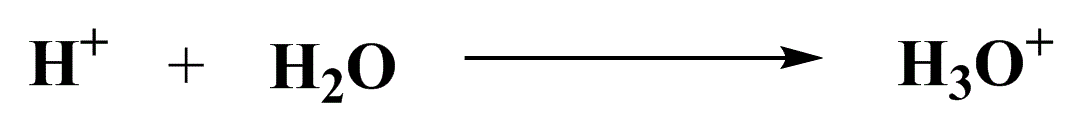
Brønsted demonstra a reciprocidade do conceito de ácido/base entre reagentes e produtos. Um ácido produz uma base conjugada associada, assim como uma base produz um ácido conjugado.
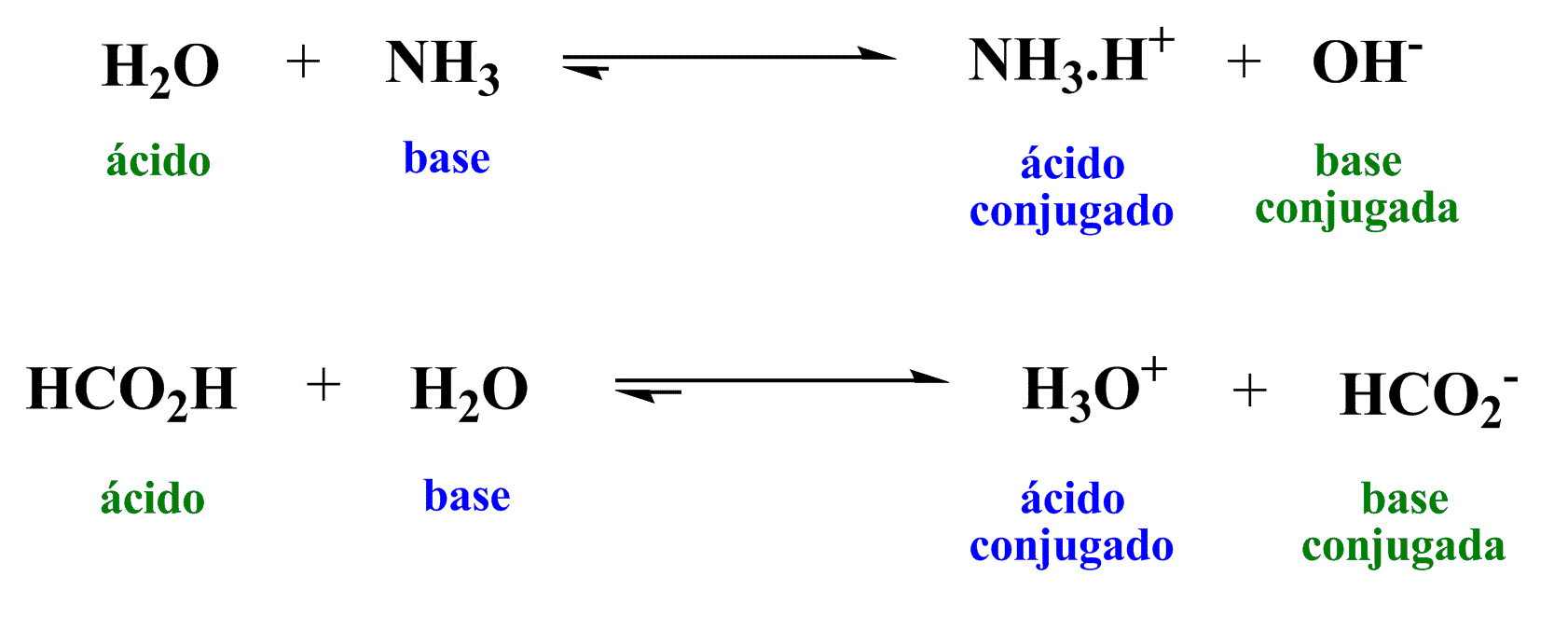
Na reação entre a amônia (base) e a água (ácido), a água protona a amônia para produzir o cátion amônio (NH4+). A notação NH3.H+ para o amônio é utilizada para melhor visualizar a receptação do H+, assim como o hidrônio poderia ser notado como H2O.H+. Como a água é mais ácida que o amônio (ácido conjugado), a reação é deslocada para formação dos produtos. É por esse motivo que o amônio se comporta como base de Arrhenius em água e o hidróxido de amônio só existe em soluções aquosas.
Na reação entre o ácido fórmico (ácido) e a água (base), são formados hidrônio (ácido conjugado) e formiato (base conjugada). Como o ácido fórmico é mais ácido que a água, ocorre a formação dos pares conjugados.
Assim, o conceito de ácido e base é relativizado e o conceito de neutralidade deixa de fazer sentido.
Referências
2 LATIMER, W. M.; RODEBUSH, W. H.; Polarity and Ionization from the Standpoint of the Lewis Theory of Valence, J. Am. Chem. Soc., Vol. 42, Nº 7, pag. 1419-1433
3 YEH, L. I.; OKUMURA, M.; MYERS, J. D.; PRICE, J. M.; LEE, Y. T.; Vibrational spectroscopy of the hydrated hydronium cluster ions H3O+.(H2O)n (n=1, 2, 3), J. Chem. Physics, Vol. 91, 7319