Por Carlos Vinícius Pinto dos Santos
Em tubo de ensaio pequeno, adicionar 10 gotas (0,5 mL) da amostra ou de solução padrão. Ao ocorrer precipitação com a adição de reagente precipitante, aguardar a deposição no fundo do tubo. Adicionar novamente o reagente ao sobrenadante límpido, até que não haja mais precipitação ou turvação. O sobrenadante é então separado do precipitado para as análises posteriores. É desejável que se utilize tubo de centrífuga, mesmo que a centrífuga não seja utilizada, uma vez que facilita a separação do precipitado.
Obs.: Uma vez que, durante a separação, são adicionados compostos com sódio, amônio e potássio, é fortemente recomendado investigar o Grupo V primeiro para evitar contaminações, ou reservar amostra original para realizar os devidos testes
Grupo V - Grupo dos Solúveis
(Na+, K+, NH4+, Mg+2)
Este grupo é formado pelos cátions que não foram precipitados nas condições de separação. Uma vez que, durante a separação são adicionados sais de sódio, amônio e potássio, é recomendado investigar este grupo primeiro para evitar contaminações. Pelo mesmo motivo, os ensaios específicos devem ser realizados em paralelo.
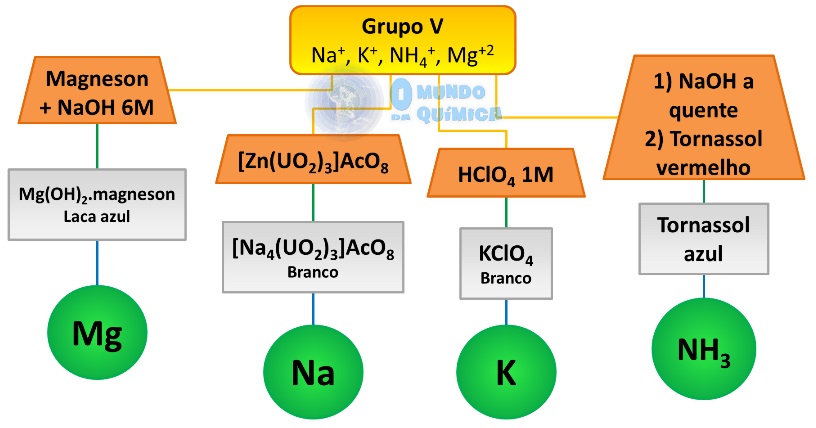
Figura 1 - Marcha de análise para o Grupo V
Identificação de Amônio
Interferentes - Não há
A adição de hidróxido de sódio, acompanhada por aquecimento, acaba por gerar amônia livre que se desprende da solução. Receber os vapores com papel tornassol vermelho umedecido com água destilada. A mudança do tornassol vermelho para azul confirma presença de amônio na amostra.
Esquema 1 - Identificação de amônio por formação de amônia em meio alcalino
Identificação de Potássio
Interferentes - Não há
Adicionar solução diluída de ácido perclórico; se ocorrer precipitação de agulhas ou sólido alongado branco há confirmação da presença de potássio.
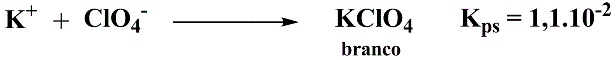
Esquema 2 - Identificação de potássio por precipitação com perclorato
Identificação de Magnésio
Interferentes - Não há
Adicionar 2 gotas de NaOH 6 M, seguido de 4 gotas do reagente reagente magneson (p-nitrobenzenoazoresorcinol). Ocorre a precipitação de hidróxido de magnésio e posterior adsorção do magneson, gerando uma laca azul que confirma a presença de magnésio.
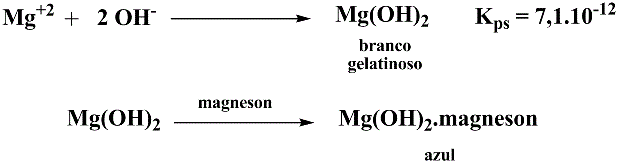
Esquema 3 - Identificação de magnésio por precipitação com magneson
Identificação de Sódio
Interferentes - lítio e potássio (ensaio com acetato de zinco e uranila); lítio e magnésio (ensaio com hexaidroxiantimoniato)
Adicionar o reagente acetato de zinco e uranila, junto com etanol. Atritar as paredes do tubo, onde a formação de pequenos cristais confirma a presença de sódio.

Esquema 4 - Identificação de sódio por precipitação com acetato de zinco e uranila
Alternativamente, é possível realizar o teste com solução aquosa de hexaidroxiantimoniato (V), proveniente da hidrólise do piroantimoniato de potássio. Magnésio e lítio interferem, de modo que os ensaios para esses cátions devem revelar sua ausência. Precipitado branco confirma presença de sódio.
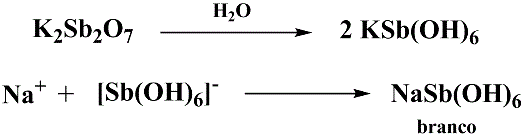
Esquema 5 - Identificação de sódio por precipitação com hexaidroxiantimoniato
Referências
1 Adaptado da apostila de Química Analítica Qualitativa Experimental, Universidade Federal do Rio de Janeiro, 2000/2
2 Arthur I. VOGEL, Vogel's Textbook of macro and semimicro qualitative inorganic analysis, 5th Edition, Longman
